薬はなぜ効かなくなるのか。原因タンパク質を分解する「CANDDY」という試み
薬はなぜ効かないのか。戦い方にあった“構造的な限界”
薬は効かないことがある。効いても、だんだん効かなくなることもある。強く効かせようとすれば、副作用も避けられない。
こうした“限界”は、これまでの薬の戦い方そのものに理由があった。サッカーに例えるなら、従来の薬はディフェンスだ。危険な選手に張り付き続けて守っていた。目を離せば、また動き出すし、強い相手にはすり抜けられてしまう。
東京理科大学発のバイオベンチャー、株式会社FuturedMeが開発する「CANDDY」(キャンディ)は、この前提を変えようとしている。マークし続けるのではなく、原因となるタンパク質そのものを細胞内で分解し、“ピッチから退場させる”。これまでの創薬が「動きを止める」戦いだったとすれば、CANDDYは「存在を消す」という別のルールで戦う。
薬はタンパク質の暴走を止める。でも止められない相手がいる
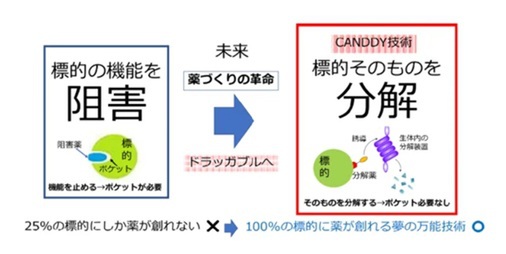
一般的な薬が狙っているのは、ほとんどの場合「タンパク質」だ。薬の多くは、暴れるタンパク質の働きを一時的に抑えることで病気をコントロールしてきた。いわば、悪さをする妖怪にお札を貼って封印するようなものだ。ただしお札が外れれば、また元通り動き出す。
さらに厄介なのは、そもそも“お札を貼れない相手”が多いことだ。タンパク質の中には、薬がしっかりとはまり込む「くぼみ」を持たないものが多く、これまで創薬の対象から外されてきた。研究者の間では、こうした標的は「Undruggable(薬にできない)」と呼ばれている。
手錠をかけて分解装置へ運ぶCANDDY
一方で、CANDDYはお札を貼るのではなく、そのスイッチ自体を消してしまう。CANDDY分子は片方で標的タンパク質を捕まえ、もう片方で細胞内の分解装置に連れていくのだ。
分解されれば、捕まえたタンパク質は消えるが、CANDDY分子自身は消費されず、次の標的へと向かう。同じ分子が繰り返し働くため、少ない量でも効果が期待できる。
長年の難敵KRASに、分解という突破口
そんなCANDDYが狙いを定めているのが、がん創薬における「聖杯」(価値が高いが、達成不可能とされる目標)とも呼ばれるKRAS(ケーラス)という標的だ。KRASは、細胞の増殖を制御するスイッチのようなタンパク質で、膵臓がんや大腸がんなど、多くのがんに関与している。
このKRASは、長年、攻略が難しい標的とされてきた。表面が滑らかで、従来の薬が入り込むための「くぼみ」をほとんど持たないためだ。しかし、CANDDYであれば、わずかな引っかかりさえあれば、そのまま分解装置へと引き渡せる可能性がある。
もしCANDDYによって、KRAS変異がんに対する有効な治療法が確立されれば、そのインパクトは大きい。同社が開発を進める候補化合物では、マウスを用いた実験において腫瘍内のKRASタンパク質の量が大きく減少し、がんの増殖を抑える結果が報告されている。
現在は、ヒトでの安全性を確認する初期の臨床試験に向けた準備が進められており、開発が順調に進めば、2030年頃に最初の承認が見込まれる。
果たして薬は“抑えるもの”から、“消すもの”へと変わるのか。創薬のルールそのものの変化に期待したい。
本記事はアフィリエイトプログラムによる収益を得ている場合があります