遺伝子のロゼッタ・ストーンに眠る可能性 ムーアの法則とスタートアップがもたらしたゲノム革命
国内の”知の最前線”から、変革の先の起こり得る未来を伝えるアスキーエキスパート。京都大学の小栁智義氏によるライフサイエンスにおけるオープンイノベーション最新動向をお届けします。
前回まではバイオ業界で始まりつつあるスタートアップ支援の仕組みについて書いたが、今回はゲノム解析業界に焦点を当てて、スタートアップ企業とその買収合戦が業界に与えたインパクトと、そこで活躍しているアントレプレナーをご紹介する。
情報処理技術の革新がもたらしたDNA解析からゲノム解析への変化
今からさかのぼること16年前の2001年、米国を中心とする国際ヒトゲノム計画によるヒトゲノム解析の最初の論文がNature誌に発表された。(http://www.nature.com/nature/journal/v409/n6822/full/409860a0.html)
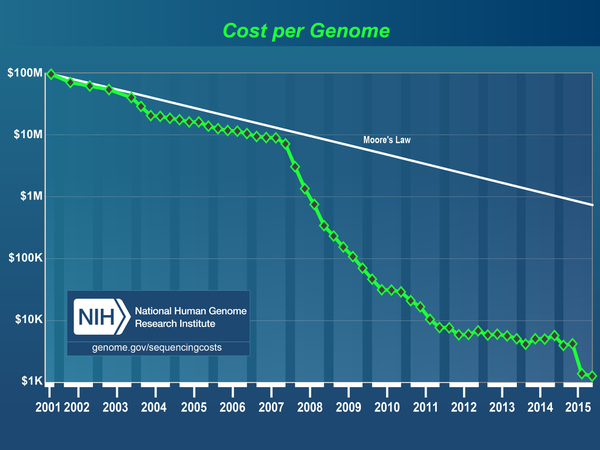
このころに使用されていたDNAシークエンサー(遺伝情報の解析方法)はいわゆる「サンガー法」と呼ばれる方法が応用されており、キャピラリーと呼ばれる細い管の中にポリマーを充填し、そこにPCR(ポリメラーゼ連鎖反応)などを駆使して前処理したDNAを流すことによって、アデニン(A)、グアニン(G)、シトシン(C)、チミン(T)という4つのDNA塩基の配列を識別していた。当時の技術でのヒト1人分のゲノム情報を解析するには、約1億米ドル(過去16年間の為替変動も加味すると、大雑把に約100億円程度)かかっていた。(https://www.genome.gov/sequencingcostsdata/)
このサンガー法の技術は、1977年に開発された方法を改良しつつ30年以上にわたって継続的なコストダウンが図られていたが、2000年前後から情報革命と半導体技術革新の波がバイオ業界にも及んできた。それまでは遺伝子も、タンパク質も、脂質も、無機物も、1つ1つの分子を丁寧に分析して生物学的な現象との関連性を研究することが主流だったのが、計算の処理速度とGUIの進化によってバイオ研究者が扱えるパソコンのレベルでも操作できる解析ソフトウエアがこのころより充実し、いわゆる「網羅的な」解析を行ない、視覚的に生物学的な現象を俯瞰できるようになってきた。同時にそれらの解析結果の1つ1つをつなぎ合わせて、巨大な分子を再構成できるようになってきた。
ヒトゲノムを読み解くロゼッタ・ストーンの発掘
2000年代半ばからは、いわゆる「次世代シーケンサー(NGS:Next Generation Sequencing)」 が普及してきた。広範囲の配列解析を一度に大量に行い、その結果を組み合わせてこれまでありえなかったような広範囲のゲノム情報を一気に取得できるようになったのである。この変化を捉えようと、2000年代後半からゲノム解析業界では新しい技術開発とスタートアップ、その技術を狙っての買収が繰り返された。本記事各段落の途中では代表的な企業を紹介していくので、興味があればチェックしてほしい。
こうして幸か不幸かゲノム解析の世界に大きな変化が起こった。かつて「DNAシークエンサー」として遺伝子を1つずつ解析していた技術は「ゲノム解析」と名を変え、一気にヒトゲノムの解析が可能なプラットフォームが整ってしまった。
情報量としては一塩基がATGCのいずれかで表現できるので2ビット、ヒトゲノムはざっくり30億塩基なので60億ビットで表現できる。つまりバイト数(8ビット=1バイト)では約750MBと認識するとどうだろうか? およそ音楽CD1枚分程度であり、今やスマホに入れ持ち歩いても容量を気にすることすらないサイズだ。
ただし実際にはこれらのAGTCの情報だけではまったく何も読み解くことはできない。これらの一見古代文字のような分子の羅列を翻訳する、ゲノム情報を読み解く「ロゼッタ・ストーン」が必要だ。まずは3万あまりと言われている遺伝子の機能を理解する必要があり、さらに近年では「マイクロRNA」やDNAのメチル化などの「エピジェネティクス」といった、ゲノムの遺伝子コード以外の機能の重要性がわかってきている。
今後もゲノムの未知の機能が発見される可能性はないとは言い切れない。新しい発見がなされるたびに、ゲノムの「ロゼッタ・ストーン」はまだ半分くらいは埋まっているのではないかと夢想している。
バイオの世界でも「ムーアの法則」
さて、そのCD1枚に入るゲノム情報の解析だが、2000年頃には100億円かかっていたコストが上述の技術革新と市場競争によって「ムーアの法則」と同じく指数関数的に下がり続けてきた。NGSの普及が始まった2007年からはさらに劇的なコストダウンが実現され、ついにはヒトゲノム1人分あたり10万円程度で解析できると言う意味で「1000ドルゲノム」とまで言われるようになった。
このころ筆者は上述のIon Torrent社を買収したライフテクノロジーズ社に勤務していたが、当時のCEOが誇らしげにこの「ゲノム解析版ムーアの法則」を解説していたことを覚えている。
「我々はゲノム解析市場の旗手としておよそ10万分の1という驚異的なコストダウンを実現した!」と市場に対してアピールしたのだが、この劇的な変化に市場自体も大きく様変わりし、結果的にライフテクノロジーズ社は基盤事業であったDNAシークエンサー事業からNGS事業への転換で起こったカニバリズムと価格破壊、そして強力な競合他社の出現に耐えきれず、現在は吸収合併を経てサーモフィッシャーサイエンティフィック社の1ブランドとなっている。
やっぱり地味(?)なバイオ業界
ところで、当時のクリントン大統領が「20世紀の科学進歩の中で最高の発見だ」と最大の賛辞を送ったこのヒトゲノム解析の成果を読者の皆さんは実感できているだろうか? 身の回りの医療状況はどうだろうか? 健康診断は変わっただろうか? 風邪薬が変わっただろうか? 我々バイオ業界の地味さがにじみ出ているところなのだが、非常に実感しにくいがじつは徐々に変化は起こりつつある。
第一に、上述のゲノム情報を読み解く「ロゼッタ・ストーン」的な役割をする基礎研究が格段に進歩し、その結果から「iPS細胞技術」や「ゲノム編集」といった、ゲノム革命以前には想像できなかった研究成果がでてきている。23&MeやDeNAのMyCodeといったゲノム解析による疾患予測は、直感的にゲノム解析のメリットを感じることができる例だ。
これらのサービスでは、過去の論文情報やアンケート情報を元に個々人のゲノムに特定の疾患のリスクを読み取り、それをレポートとして返してくれる。ただし医療として確定診断はできないので、あくまでも病気のなりやすさの指標を示して健康維持に役立てる情報を提供するという立て付けだ。
また、同じく遺伝子検査ながらまったく違うゲノムを対象としているのが、腸内フローラをゲノム解析で解析するベンチャー企業、サイキンソーのサービスだ。腸内に生息している多種多様の細菌群(細菌叢――「さいきんそう」と読む)を「メタゲノム解析」と呼ばれる方法で一気に解析し、生息している細菌の種類から推測される顧客の腸の状態を医師や顧客自身へレポートする。このメタゲノム解析という手法ではもはや生物種を1つ1つ分けることなく、一気にゲノムを分離して解析してしまってから、どんな細菌がどんな割合で生息しているかを識別する。
がんの検査にもゲノム解析が
NGSの技術の特徴を活かした、より医療の現場に近いサービスもでてきている。がんの遺伝子検査サービスだ。
がんという病気は、人間の体内にある細胞の遺伝子が何らかの原因で傷つくことで暴走し、特定の種類の細胞ばかりが増殖するという特徴を持っている。また多くの場合、通常の細胞の持つ遺伝子の修復機能が減退しているので、複数種類の遺伝子変異が1つのがん組織に含まれていることも珍しくない。もちろんその周辺には正常組織も含まれているので、これまでの遺伝子検査法ではよく知られているごく一部の特定の遺伝子変異についてしか検出ができなかった。
だがNGS技術の進展により、正常細胞に紛れ込んでいるがん細胞の不特定多数の遺伝子変異についても検出することができるようになってきた。米国のFoundation Medicine社では、このように一般にあまり知られていない遺伝子変異を持つがんに対しても分析を実施し、抗がん剤の選択に役立つ情報を提供するサービスを行なっている。このサービスを利用すると、通常の検査では見つけることができなかった適切な抗がん剤が見つかる可能性がある。
同社は、2015年に世界的な製薬企業であるロシュ社が1000億円以上を出資して子会社化したことからも、業界の期待がうかがえる。ゲノム解析によるがん検査領域では、筆者の所属する京都大学でも2015年4月よりOncoPrimeという名称で日本初の「がんゲノム検査サービス」の提供を始めている。
日本発のゲノム解析ブレイクスルーの可能性
さて、冒頭の国際ヒトゲノム計画によるゲノム解析だが、実はこの計画と並行して1人のアグレッシブな研究者、と言うよりは起業家によってもう一方のヒトゲノム解析の最初の論文がScience誌から発表されている。 (http://science.sciencemag.org/content/291/5507/1304)
Craig Venter博士が立ち上げたセレラ・ジェノミクス社は当時巨額の資金調達を行ない、国際ヒトゲノム計画が途中まで仕上げていた公開情報をも使って一気に追い上げ、追い越しそうになっていたのだ。結果的に双方が同時に論文を発表をすることにはなったが、Venter博士の存在が国際ヒトゲノム計画を加速したと捉えている人は多い。
そして起業家によるゲノム技術革新が日本からも起ころうとしている。大阪大学産業科学研究所の川合知二特任教授の技術を元に創業し、本藏俊彦氏が率いるクオンタムバイオシステムズ社は、上述のNGSのさらに先を行く「1分子電流計測」という技術でブレイクスルーを起こそうとしている。
この一分子電流計測技術は、一本のDNA鎖中の単一塩基が持っている電気的な特性を、ナノサイズの穴を通す際にイオン電流として計測する技術であり、イギリスのオックスフォード・ナノポア・テクノロジーズ社が「USBサイズの使い捨てシークエンサーを実現する!」という触れ込みで話題をさらってきた。分析精度の面で課題があるものの昨年末に製品化に漕ぎ着け、競合他社を一歩リードしている。
これに対してクオンタムバイオシステムズ社は、DNAの「トンネル電流」を計測することでより正確な一分子電流計測を技術的には実現しており、製品化が待たれる。実は筆者は、川合教授が所長も務めた産業科学研究所で学生時代を過ごし、川合研の学生と共にDNAを使った実験を行なっていた。当時はまったく理解できなかった技術が20年近く経って一気に花開いてきており、科学技術発展のインパクトを実感している。
NGSで過去10年の間に革命的に変わったゲノム解析の世界はここに来て新しい局面を迎えており、約750MBのゲノム情報のダイナミクスにはまだまだ新しい情報が隠れているに違いない。新たなロゼッタ・ストーンのピースの発見が楽しみだ。
バイオとスタートアップの都合の良い関係
今回紹介したゲノム解析技術はほとんどが、大学やスタートアップ企業から生まれてきている。「未知の部分が大きい」という技術的な未熟さの一方で「人の生命・健康に関わる」という大きなニーズが存在するという、商業的には大きなギャップが存在している。このギャップを埋めるために基礎的な科学的発見を比較的「生」に近い状態でも製品、サービスとして成立するのだが、初期の投資には当然大きなリスクが伴う。
これはiPS細胞や再生医療関連の事業とも似通っており、多くの場合で事業化の際にターゲットとする市場が固まっていなかったり、市場の想定ができても製品のイメージを作り込むことが難しい。従って、中長期的な計画に従って製品開発をする大企業よりは、アントレプレナーの属人的な能力に頼って会社の成長とともに技術、そして市場を立ち上げていくスタートアップ的なパターンが根強いのだろう。
また一方で生活必需品ではないために、自動車や電化製品と異なり常に最新の技術を持つ新製品を生み出し続ける必要がある。そのために大企業が将来予測をして特定の基礎研究から製品化に成功することは少なく、結果として買収によって製品ポートフォリオを更新し続けているという状況があり、スタートアップの優位性を後押ししている。
Craig Venter博士、Jonathan Rothberg氏、本藏俊彦氏を始め、在野の多くのアントレプレナーが科学の世界から「生」の技術を新鮮なうちに世界に普及するためにスタートアップの仕組みを利用しており、その流れは日本にも広まっている。今回はゲノム解析技術と情報革命の接点でのビジネスを紹介したが、ゲノム以外でも思ってもみないバイオ技術と情報産業の組み合わせが可能かもしれない。
ぜひ読者の皆さんもバイオ技術者と交流して、生命の神秘を読み解くロゼッタ・ストーン発掘に参加してほしい。来る8月4日、京都リサーチパークにおいてHealthcare Venture Conferenceの開催を予定している。筆者も登壇し、京都を通じて日本の技術を海外へアピールする場として育てようとしている。できるだけわかりやすく、海外のトレンドも交えながらバイオ系のベンチャーの活動紹介を予定しているので、真夏の暑い京都で熱い議論を交わしていただきたい。
アスキーエキスパート筆者紹介─小栁智義(こやなぎともよし)

博士(理学) 京都大学大学院医学研究科「医学領域」産学連携推進機構 特定准教授。より健康で豊かな社会の実現を目指し、大学発ベンチャーを通じたライフサイエンス分野の基礎技術の実用化、商業化に取り組んでいる。スタンフォード大学医学部での博士研究員時代にベンチャー起業を通じた研究成果の事業化に接し、バイオビジネスでのキャリアを選択。帰国後は多国籍企業での営業/マーケティング、創薬、再生医療ベンチャーでの事業開発職を歴任。現在は大学の産学連携業務に従事し、国立研究開発法人日本医療研究開発機構「創薬技術シーズの実用化に関するエコシステム構築のための調査研究事業」分担研究代表者も務める。経済産業省プログラム「始動Next Innovator」第1期生。大阪大学大学院卒。
本記事はアフィリエイトプログラムによる収益を得ている場合があります