規制当局への副作用報告形式の新規格「E2B(R3)」に対応
キヤノンITSが「EDI-Master DEX for Medical」新版を発売
2016年09月27日 10時00分更新
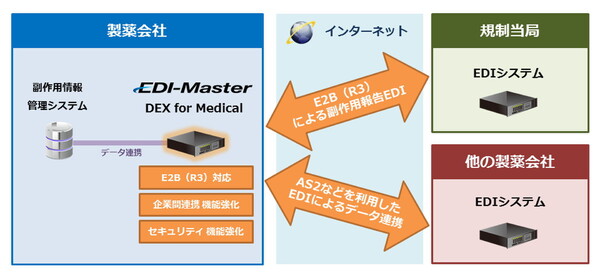
キヤノンITソリューションズ(キヤノンITS)は9月27日、製薬企業向けEDIシステム「EDI-Master DEX for Medical」の新版(バージョン5)を発売した。PMDA(医薬品医療機器総合機構)に対する副作用報告形式の新規格「E2B(R3)」に対応した。
EDI-Master DEX for Medicalは、製薬企業と規制当局(PMDA/厚生労働省)の間で行われる医薬品等の副作用報告を電子的に行うためのEDIシステム。80社を超える製薬企業で導入実績がある。
今回のバージョンアップでは、従来からのE2B(R2)に加えて、今年4月から運用が始まっているE2B(R3)にも対応した。製薬企業がこれを利用することで、R2/R3の並行運用期間(2019年3月まで)中に、確実に移行を完了できる。
さらに、グループ会社やパートナー企業など、他の製薬会社との間でのデータ連携機能を強化したほか、IPAガイドラインに基づくセキュリティレベル設定機能の追加、NSA(米国国家安全保障局)の「Suite B」暗号方式に対応している。
価格は700万円(税別)から。キヤノンITSでは、2020年までに製薬企業を中心とする累計100社のシステム構築/導入を獲得し、EDIソリューション関連事業において年間売上高25億円を目指すとしている。
本記事はアフィリエイトプログラムによる収益を得ている場合があります