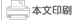慶應義塾大学医学部/国立成育医療研究センター/かずさDNA研究所/テンクー/DNAチップ研究所ら研究グループは7月17日、ヒト胚性幹細胞(Embryonic Stem:ヒトES細胞)を使って幹細胞の分化に影響する転写因子(transcription factor:TF)の網羅・同定に成功した事を発表した。
研究の結果は公的データベースと慶応義塾大学ウェブサイト上で公開されると同時に、遺伝子誘導可能なヒトES細胞も研究者に提供される。各データ・材料リソースはヒト遺伝子の機能を解析したものの中で最大規模であり、幹細胞研究とTFの機能解明に役立つ事が期待される。
ES細胞は胚盤胞に移植する事であらゆる臓器に分化する細胞であり、人工多能性幹(induced pluripotent:iPS細胞)細胞とともに多能性幹細胞として知られている。一部の細胞・組織では臨床研究が開始されているものの、目的とする細胞への分化を制御する因子が不鮮明な場合が多く、一部の細胞作成に応用されるだけに留まっている。
また、マウス等による先行研究においてTFは細胞の分化結果に大きな役割を持つ事が判明していたものの、ヒトについては体型的な大規模研究が行われておらず、TFと細胞運命の因果関係の多くが不明なままとなっていた。
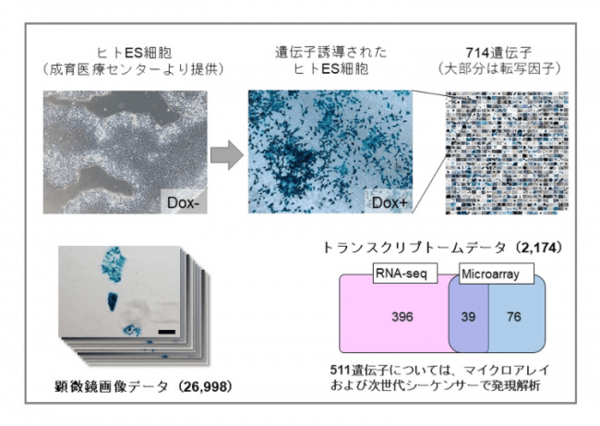
今回の研究では、薬剤による制御が可能な遺伝子を組み込んだヒトES細胞株を樹立。714遺伝子を対象にした2万6998の顕微鏡画像と、511遺伝子の48時間経過後の遺伝子発現データの取得に成功。
これらを解析したところ、ゲノム中のほとんどの遺伝子は511によって制御されており、従来は誘導が困難とされるヘテロクロマチン中の遺伝子も特定のTFにより発現の誘導が可能である事が判明した。
また、これらのデータをヒトの臓器細胞の遺伝子発現データ(公共データベースより取得)と比較したところ、ヒトの各臓器と類似性の高い状態を誘導するTFの同定に至った。
今回の研究で得られた生物ビッグデータは転写因子を同一プラットフォームで誘導しており、人工知能などによる数理的な解析に適している。今後、複雑なTF同士のネットワーク構造の解明が進む事により、iPS細胞を始めとしたヒト幹細胞から任意の細胞系譜を自在に生み出す技術開発に繋がる可能性が期待される。
本記事はアフィリエイトプログラムによる収益を得ている場合があります