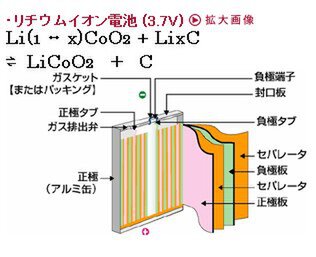
そもそも、リチウムイオン電池って?
ところで、リチウムイオン電池の前にも、充電ができるいわゆる二次電池はいくつかあった。乾電池で使われる、ニッケルカドミウム(ニッカド)電池や、同じく乾電池やパソコンで使われるニッケル水素電池などである。これらに比べ、リチウムイオン電池は、電池としての容量が大きく、ひとつの発電ユニット(セル)あたりでも3.6Vと、それまでの電池と比べ3倍ほど高い電圧を発生する。これにより、例えばパソコンで利用するなら、より長時間の駆動が可能になり、携帯なら、いっそうの小型化に寄与してきた。また、充放電を繰り返すと発生する、電圧が低下する「メモリ効果」が原理的にはなく、性能低下も少ない。
半面、リチウムイオン電池は充放電の管理が難しく、温度、電圧、電流などを細かにコントロールして充放電する必要がある。それを守らないとどうなるかというと、簡単にいって発火するのだ。
難しくいうと、リチウムイオン電池に利用されるリチウムという物質は、水と反応すると水素(=燃えやすい、簡単に爆発する)を発生するので危ない。そのため水ではなく有機溶剤を電解液に使用している。これが高電圧を発生する要でもあるのだが、過充電を行なうと、負極に電解液中に溶けたリチウムイオンがくっつきすぎて、金属リチウムとして成長する。これが針みたいな役割をはたし、負極と正極の間にあるセパレーターと呼ばれる絶縁シートを突き破り短絡(ショート)してしまう。すると当然そこで発熱が起こり、正極のリチウムを含んだリチウム金属酸化物の結晶が崩壊。次々にリチウムを放出する“熱暴走”と呼ばれる事態に発展する。まるで臨界突破のようなイメージだ。悪いことに、高電圧をもたらしてくれた有機溶剤というのはシンナーに代表されるように、よく揮発し、よく爆発する性質をもつから、さあたいへん。リチウム金属酸化物は酸化物なので、崩壊すると酸素を放出するらしいし。さあ、これで役者はそろった、5秒前。4、3……。
と、このように、リチウムイオン電池は、ルールを守らないで使うと、簡単に発火する。このため、リチウムイオン電池を使ったバッテリーユニットの中には、常に個々の電池の温度を監視するセンサーや、過電流監視センサーなどが組み込まれ、パソコンや携帯電話側、または充電器で充放電をコントロールするようになっている。これによりリチウムイオン電池はそうそう発火したりするものではないが、逆にいえば、製品付属のものでない充電器を使ったり、メーカー製でない電池を使うと、例えば中国でいくつか報道されていたような携帯電話の炎上、ということにもなりかねない。同様に、たとえ正しい充電方法をしていたとしても、バッテリーに衝撃を与えたり傷つけると、絶縁のセパレーターが破損してショートが発生。あるいは使用する温度条件によっては、それだけで熱暴走が発生する可能性も否定できない。メーカーが正しい充電法や使用法を勧めているのには、こんな理由がある。
(次ページへ続く)