 消費者庁は2日、食品表示の新たな制度「機能性表示食品制度」のガイドライン案を公表し、都内で説明会を開催した。同制度では、一定の条件を満たした上で科学的根拠を消費者庁に届け出れば、企業の自己責任で健康食品などの食品に機能性が表示できるようになる。機能性を表示した「機能性表示食品」は、最短で6月から市場に流通する見込み。
消費者庁は2日、食品表示の新たな制度「機能性表示食品制度」のガイドライン案を公表し、都内で説明会を開催した。同制度では、一定の条件を満たした上で科学的根拠を消費者庁に届け出れば、企業の自己責任で健康食品などの食品に機能性が表示できるようになる。機能性を表示した「機能性表示食品」は、最短で6月から市場に流通する見込み。
「機能性表示食品」は、病気に罹患している人は対象外で、未成年者・妊産婦・授乳婦を除く健康な人と健康でも病気でもない境界域に入る人を対象としている。表示できる条件は、製品に配合されている機能性関与成分が明確であること、安全性の根拠・機能性の根拠が説明できること、食事摂取基準が定められた栄養素(ビタミン・ミネラルなど)でないこと、健康被害の情報収集体制を整えていること、容器包装に適正な表示が行われていることなど。
販売の60日前に必要書類を届け出た後、消費者庁が提出資料に不備がないか、疾病名など「NGワード」が入っていないかなどの形式的な審査を行い、審査を通過すれば機能性を表示した食品が販売できるようになる。届出の情報は、企業秘密に関連する内容を省き、消費者庁がネットで公開する。
機能性の根拠となる説明資料は、最終製品による臨床試験か、最終試験または機能性関与成分に関する研究レビュー(システマティック・レビュー)のいずれかが必要となる。機能性表示の文言には、機能性の根拠に臨床試験か研究レビューのどちらを利用しているかを明確にすることが求められた。研究レビューによる根拠の場合、「報告されている」ということを明確にしなければならず、「本品にはA(機能性関与成分)が含まれます。AにはBの機能があることが報告されています(機能性)」といった具体例を示した。届出で審査を通過した表現は、通販などの広告でも使用できる。
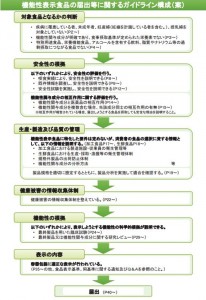
ガイドライン案には、新制度に対応できるのかを確認できるようにした届出のフローチャートや、研究レビューの考え方や手順の例、提出資料のフォーマット(サンプル)なども添付され、新制度に対応する準備の詳細情報が整った。ガイドラインの正式版は近日中に発表予定(消費者庁の担当官)としたが、残りの作業は細かい文章の修正などで、ガイドライン案の内容は大きく変わらない見込み。届出の受付は、食品表示法が施行される4月1日以降に開始する予定。最短で6月に機能性表示食品が市場に流通する。